【3.4.5.3】溶剂化
建议先阅读:
溶剂化,即溶剂分子结合溶质离子的过程。分子间作用力主要有四种:取向力、诱导力、色散力以及氢键。名称虽多,简单来说,就是分子具有偶极矩,无论是永久性的还是振动引起,它都会导致分子内部正负电荷中心分离。那么,在离子电场的影响下,这些正负电荷分离的“东西”就是吸附在离子周围,这个过程被称为溶剂化。其它的名称还有,溶剂化作用、溶剂化效应等等。
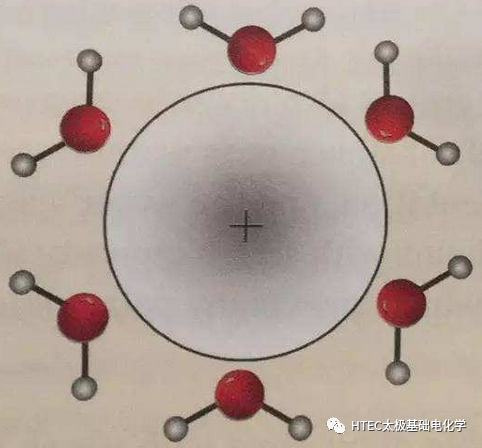
除了偶极矩的原因之外,氢键也是一种很重要的分子间作用力,它也是溶剂化形成的原因之一。氢键形成规律很容易记忆,活性氢与强电负性原子之间的就可能存在氢键。活性氢就是电子易脱离的氢原子,比如O-H或N-H等等。

一、溶剂化介绍
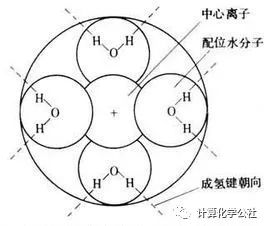
在分子动力学模拟中,探究体系的结构变化至关重要,溶剂化效应对反应影响的关注历史悠久。不同的溶剂可以影响反应速率,甚至改变反应进程和机理,得到不同的产物;溶剂对反应速率的影响十分复杂,包括反应介质中的离解作用、传能和传质、介电效应等物理作用和化学作用,溶剂参与催化、或者直接参与反应(有人不赞成将溶剂参与反应称作溶剂效应)。溶剂化作用是溶剂分子通过它们与离子的相互作用,而累积在离子周围的过程。该过程形成离子与溶剂分子的络合物,并放出大量的热。溶剂化作用改变了溶剂和离子的结构,溶剂化作用也是高分子和溶剂分子上的基团能够相互吸引,从而促进聚合物的溶解。下图为一个经典的溶剂化结构示意图。
参考资料
药企,独角兽,苏州。团队长期招人,感兴趣的都可以发邮件聊聊:tiehan@sina.cn
![]() 个人公众号,比较懒,很少更新,可以在上面提问题,如果回复不及时,可发邮件给我: tiehan@sina.cn
个人公众号,比较懒,很少更新,可以在上面提问题,如果回复不及时,可发邮件给我: tiehan@sina.cn

