【3.1】十二种可以治愈癌症的免疫治疗药物
免疫T细胞可以杀死癌细胞。癌症疫苗通过增加免疫 T 细胞的数量发挥作用。对免疫系统施加了极其严格的生物学限制,以防止过度的 T 细胞激活和扩张。同样的生物学限制也限制了癌症疫苗。
已经发明并配制了绕过生物学限制的免疫治疗剂,包括:
- 树突细胞激活剂和生长因子
- 疫苗佐剂
- T细胞刺激剂和生长因子
- 免疫检查点抑制剂
- 中和或抑制抑制性细胞、细胞因子和酶的试剂。
本综述重点关注 12 种药物,所有药物均具有增强 T 细胞反应的能力。单独来说,每个人都几乎没有机会在癌症治疗中取得实质性进展。在生物学决定的组合中,这些药剂极有可能产生影响。这些药物未来可用于开发创新的联合癌症治疗方案,将为国家癌症治疗转化研究企业的决心提供一个基准。
一、前言
免疫 T 细胞数量和功能都是疫苗功效的重要组成部分。疗效不仅与 T 细胞的数量有关,还与 T 细胞持续存在的时间长度有关,即在药理学术语中,即“曲线下面积”。
癌症疫苗将抗原呈递给少数能够“识别和响应”抗原的 T 细胞,从而刺激它们增殖并增加数量。对免疫系统施加了极其严格的生物学限制,以防止 T 细胞过度扩张。许多允许 T 细胞活化和数量增加的成分和因素已被鉴定并构建为免疫治疗剂。类似地,许多阻止免疫效应细胞激活、扩增或持续存在的成分和因素已被确定,并且干扰这种禁用的药剂也已被构建为免疫治疗剂
可以将癌症疫苗从有趣的生物学现象转化为有效治疗剂的药剂包括:
- T 细胞生长因子可增加幼稚 T 细胞的数量和库
- 增加树突细胞 (DC) 数量的生长因子
- 激活 DC 和其他抗原呈递细胞 (APC) 的激动剂
- 允许和增加癌症疫苗的佐剂
- 激活和刺激 T 细胞的激动剂
- T 细胞检查点阻断抑制剂
- T细胞生长因子增加免疫T细胞的生长和存活
- 抑制、阻断或中和癌细胞和免疫细胞衍生的免疫抑制细胞因子的药剂
二、缺乏广泛的免疫治疗药物:佐剂示例
当今免疫治疗面临的主要问题不再是缺乏知识或缺乏具有经证实免疫作用的药物,而是缺乏具有已证实免疫功能的药物的广泛可用性。佐剂的例子说明了这个问题。关于疫苗有一个“普遍真理”:需要佐剂来实现最高水平的免疫反应。尽管有这个普遍真理,但很少有疫苗佐剂可用于广泛的测试。问题是“为什么没有佐剂可用?” 美国国家癌症研究所 (NCI)、食品和药物管理局 (FDA) 和工业界都发挥了作用。
NCI 和其他资助机构已经花费了数亿甚至数十亿美元用于癌症疫苗开发。用于基本疫苗成分的支出很少。人们普遍认为,需要佐剂来实现最高水平的免疫反应,但还没有协调一致的努力来确保适当的佐剂可用,即使是正在进行的 NCI 资助的癌症疫苗试验也是如此。
根据 FDA 的政策和习惯,佐剂仅被批准为疫苗的成分。因此,学术界使用的最常见的佐剂是批准用于非佐剂目的的药剂。粒细胞-巨噬细胞集落刺激因子 (GM-CSF) 常用于学术疫苗试验,部分原因是它很容易获得。GM-CSF 被 FDA 批准作为造血生长因子,而不是作为疫苗佐剂。如果 GM-CSF 仅作为佐剂具有活性,它就不能用于癌症疫苗的测试。同样,咪喹莫特,一种被批准用于治疗生殖器疣和浅表基底细胞癌的药物,而不是作为佐剂,开始在 NCI 资助的癌症疫苗试验中用作佐剂。“Catch 22”是批准用于非佐剂目的的佐剂是广泛可用的,而,无论效力如何,仅起佐剂作用的佐剂都不是广泛可用的。罗伯特·卡皮齐 (Robert Capizzi) 观察到,“大部分抗癌药物开发都在批准后进行”。佐剂未被批准作为佐剂,因此不能用于癌症药物开发。对于不能作为单一疗法有效的佐剂的广泛测试和批准,FDA 没有给出明确的前进道路。
行业决策是由“市场的无形之手”驱动的。理性决策是基于监管和商业考虑做出的。拥有强大佐剂的公司倾向于将它们开发为单一疗法,例如 CpG 和白细胞介素-12 (IL-12)。具有辅助潜力但作为单一疗法失败的药物通常“被搁置”,因为公司没有看到清晰合理的监管和商业前进道路。
三、NCI免疫治疗剂研讨会对具有高潜力作为免疫治疗药物的药物进行排名
NCI 迈出了一小步,开发了一份具有高潜力作为免疫治疗药物的药物排名列表。 Cheever MA, Creekmore S eds. National Cancer Institute Agent Workshop Proceedings: July 12, 2007. http://web.ncifcrf.gov/research/brb/workshops.asp
表 1. 用于治疗癌症的高潜力药物的排名
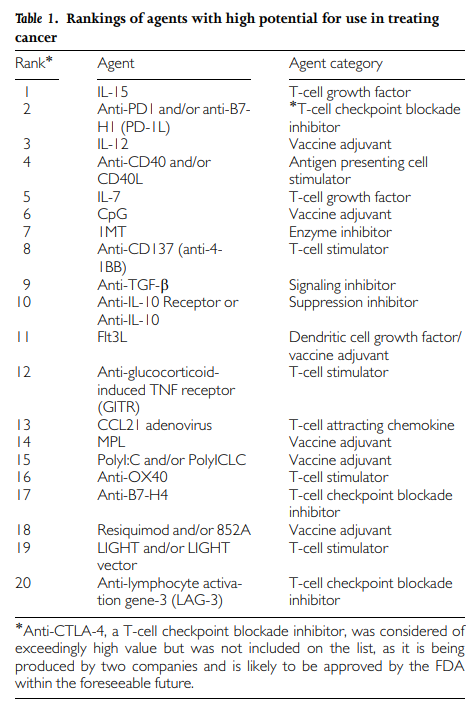
用于列入排名列表的标准包括:
- 用于癌症治疗的潜力
- 多个独立临床研究人员的感知需求
- 在不止一种临床环境中的潜在用途,即针对不同的肿瘤类型或作为多种治疗方案的一部分,
- 不能广泛用于患者测试。
未使用的标准包括:
- 先前失败的商业化尝试
- 知识产权
本综述重点关注列表中已证明免疫疗效且已进行临床试验或即将进入临床试验的 12 种药物

具体的介绍,见其博文。
结论
在体内将 T 细胞水平提高到非凡水平所需的工具就在眼前。所描述的 12 种药物均已证明能够显着增加特定的 T 细胞反应。单独使用这些药物几乎没有机会在癌症治疗中取得实质性进展。总之,在创新和智能的组合中,代理极有可能产生影响。
想象一下用 IL-7 连续治疗癌症患者以增加初始 T 细胞的数量和库,Flt3 增加 DC 的总体负荷,抗 CD40 激活 DC,一种多价癌症疫苗与 IL-12 的组合, CpG, MPL, polyI:C 和 resiquimod 佐剂激活和诱导癌症免疫 T 细胞的增殖, 4-1-BB 进一步刺激免疫 T 细胞的激活和增殖, anti-PD1 抑制 T 细胞检查点封锁, IL-15 维持免疫 T 细胞的增殖和存活,1MT 抑制 IDO 的免疫抑制。可达到的免疫 T 细胞数量应该使体内环境非常不适合癌细胞。如果这还不够,那么直接在体外扩增肿瘤免疫 T 细胞并在体内转移它们以达到更大的数量。
上述情况充满困难,但利用当今的技术,开发包括使用标准癌症疗法在内的生物定向多组分免疫治疗方案是完全可行的。科学发现就在眼前。应用已经发现的免疫治疗剂本质上是一项工程壮举。免疫学科学界在开发 T 细胞免疫反应的原理方面做了非凡的工作。学术界和工业界的临床前科学家联合开发了诱导和大大增强免疫 T 细胞反应所需的免疫治疗药物。将免疫学的所有原理应用到使用近在咫尺的免疫治疗药物治疗癌症的时机已经成熟。优先事项已由广泛的免疫治疗社区确定 (12)。
具有作为免疫治疗药物潜力的药物清单(表 1)包含八种额外的药物,每种药物都有很大的潜力:信号抑制剂、抗转化生长因子-β;一种免疫抑制抑制剂,抗 IL-10 受体;三种 T 细胞刺激剂,抗糖皮质激素诱导的 TNF 受体,抗 OX40 和 LIGHT; T 细胞吸引趋化因子,CCL21;和两种 T 细胞检查点阻断抑制剂,抗 B7-H4 和抗淋巴细胞激活基因 3。完全有理由认为这些agent以及其他正在开发的代理将被证明与本综述中描述的 12 种代理一样有效。
参考资料
- 2008,Twelve immunotherapy drugs that could cure cancers 。 https://onlinelibrary.wiley.com/doi/10.1111/j.1600-065X.2008.00604.x
