【5.1.1】肿瘤突变负荷(TMB, tumor mutational burden))
- TMB 是肿瘤组织 DNA 中基因组体细胞突变数的指数, 它是测量肿瘤细胞内编码蛋白的平均每百万碱基(1Mb)范 围内的非同义碱基突变数量,包括基因编码错误、碱基替换、 基因插入或缺失等各种形式的突变。
- 高 TMB 患者对于免疫 检查点抑制剂疗效可能更好,同时需考虑肿瘤发生部位,以 及 CD8+细胞与新抗原的表达等情况。
作为现代癌症治疗的新支柱,免疫肿瘤学正在彻底改变癌症治疗。免疫检查点抑制剂(Immune checkpoint inhibitors, ICI),包括抗PD-1和抗PD-L1等,通过释放免疫系统抗肿瘤反应的制动作用来发挥作用。尽管ICI疗法取得了突破性的进展,但它并非没有副作用,也不是在所有患者中都具有理想的疗效。因此,人们非常想找到可以识别对ICI治疗有良好反应的生物标志物。目前在临床上使用的生物标记包括PD-L1免疫组化以及微卫星高不稳定性(microsatellite instability–high, MSI-H)或错配修复缺陷(mismatch repair deficiency, dMMR)。
在2017年获得美国食品药品监督管理局批准pembrolizumab(anti-PD-1)可以用于晚期MSI-H / dMMR实体瘤,无论其肿瘤类型如何,这些肿瘤均在先前的治疗后进展。这是美国食品药品管理局首次批准与肿瘤类型无关的分子生物标记物。最后,尽管PD-L1和MSI-H / dMMR均已被确定为预测ICI反应的标志物。但它们仍非完美,其灵敏度和特异性均不佳。因此,需要继续寻求更好的ICI治疗反应预测,其中一种新兴的生物标志物就是肿瘤突变负荷(tumor mutational burden, TMB)。
简而言之,TMB是肿瘤内存在的突变数。由于许多使用该生物标记物的原始研究都是基于外显子测序计算的,因此通常将其视为基因组(外显子组)编码区内存在的突变数。但是,由于用于计算TMB的测试方法已经扩展到各种靶向基因测序面板(gene sequencing panels),其覆盖范围远小于全外显子组。所以TMB通常被报道为存在于1Mb中的突变数(计算公式即:
突变个数/检测的外显子Mb长度
正是因为不同的平台可能涵盖不同数量的基因,所以当比较不同测试方法和平台的TMB值时,这个数字最具信息量。
关于测序panel的解释。临床进行基因检测的时候,并不是检测所有基因的突变。而是人为的选择多个重要的基因来进行检测。例如之前介绍的MKSCC就是一个基因panel。这个panel检测了468个基因的基因组的变化。
二、TMB作为biomarker的原理
目前市面上的检测方法是指患者靶向测序编码区每百万碱基(Mb)的体细胞突变数目,包括点突变和插入缺失。体细胞的非同义突变可表现为RNA和蛋白水平的变化,产生的新抗原(或新表位)、蛋白片段/肽段等被自身免疫系统识别为非自身抗原,激活T细胞,引起免疫反应。
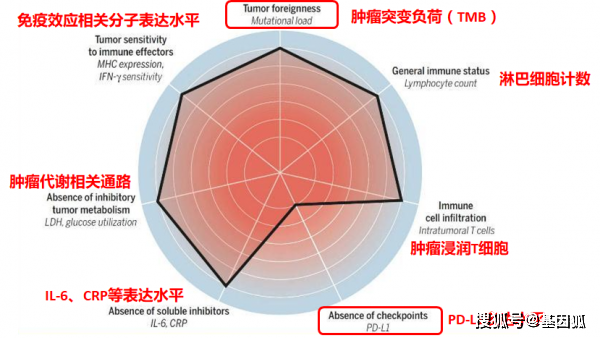
T细胞活化通路中多个因素可能是免疫治疗潜在Biomarker
使用MSI-H/dMMR和TMB作为ICI生物标志物的原理是相似的:大量的突变产生大量的改变肽,其中的一部分被主要组织相容性复合体(major histocompatibility complex)成功表达和处理,从而产生新的抗原,免疫系统可以对其产生抗肿瘤反应(图1)。因此,存在的DNA突变越多,就会产生越多的候选多肽,从而导致新抗原被免疫系统成功识别的可能性更高。因此,MSI-H/dMMR和高TMB的肿瘤之间存在重叠。然而,值得注意的是,尽管许多MSI-H/dMMR肿瘤也有高TMB,但很大比例的TMB高肿瘤在MMR内没有缺陷

在患者免疫功能正常的情况下,影响I-O药物疗效核心的因素有两个:
- 肿瘤细胞表面的新抗原数量是否足够多,以致肿瘤细胞能被免疫细胞正确识别;
- 肿瘤细胞是通过PD-1/PD-L1这类配体抑制了免疫系统活性,而PD-1/PD-L1这类抗体药能解除这种抑制状态;

除了MSI-H / dMMR肿瘤外,在成人实体瘤中往往会观察到高TMB值,这与环境暴露有关,例如肺癌和膀胱癌中的吸烟和黑色素瘤中的紫外线暴露。子宫内膜癌和结肠癌当中的一种具有致病性的POLE突变虽然发病比较少,但是具有较高的TMB。在不同的肿瘤类型之间以及在相同的肿瘤类型内,TMB值都可以有很大差异。此外,尽管不是所有的肿瘤类型的TMB都高,但是总会有几个TMB高的患者。因此与MSI-H / dMMR生物标志物类似,由于其具有肿瘤不可预知的适应症,TMB也是有望在多种肿瘤类型中作为生物标志物使用。
TMB检测存在题注意事项:
- 第一,TMB有别于PD-L1表达, PD-L1表达低的病人不一定TMB低,也可能存在TMB高的情况,在未来研究中,TMB和PD-L1同时检测是非常必要的。
- 第二,目前涉及TMB检测的研究均为回顾性研究,亟需前瞻性的临床研究来进一步落实TMB的真正作用。
- 第三,相比于PD-L1的检测,TMB检测有自身不足的地方,TMB检测需要的组织量相对较多,并且需要用二代测序做检测,耗时比较长,耗费也比较高。
在几种肿瘤类型中,高TMB与对ICI的反应有关。例如,在接受nivolumab和ipilimumab治疗的患者中,不管PD-L1的表达如何,人们发现高TMB与非小细胞肺癌(NSCLC)显著改善无进展存活率有关。这也提供了TMB和PD-L1可能作为独立生物标志物的证据。TMB作为生物标志物的用途不仅限于NSCLC,因为有证据表明TMB还是头颈癌和膀胱癌患者ICI治疗的预测性生物标志物。虽然TMB是有前途的ICI治疗的指标,但是如果要广泛应用于各种肿瘤类型时,必须谨慎。因为已经证明一些肿瘤的反应比基于TMB预测的要好,而其他肿瘤的反应比基于TMB预测的要差。由于对TMB缺乏共识和标准化,目前还不清楚不同的肿瘤类型是否应该有不同的临界值来分类为高TMB和低TMB。例如在上述NSCLC当中TMB的cutoff值是10。而在其他研究中,临界值是基于特定肿瘤类型和队列的中位数确定的。
如前所述,TMB检测的金标准是对肿瘤和匹配的“正常”组织进行全外显子测序,以去除生殖系变异。然而,对于许多临床实验室而言,这既昂贵又困难。因此,一些研究小组已经证明,相当稳健的TMB计算可以从包含足够数量的靶向癌症基因面板(panel)当中计算获得,我们也可以期望,对于常规基因分型分析来说足够的相同标本类型也将适用于TMB计算。例如,许多细胞学标本通常被成功地用于各种分子诊断应用,如果肿瘤纯度足够高,则有望在TMB计算中表现出同样好的表现。
这里简单说一下所谓的生殖系的变异。人类的染色体首先是基于孟德尔遗传获得自父母的。所以从父母传到本身的变异就是生殖系的变异。肿瘤发生的时候会产生新的变异,这里通过检测肿瘤组织和正常组织,来确定哪些是肿瘤发生过程中产生的变异。
四、TMB分级
分类方法1:
将TMB划分为以下3个层级
low TMB : 1-5 mutations/mb
intermediate TMB : 6-19 mutations/mb
high TMB : > 20 mutations/mb
分类方法2
按照在受检者瘤种中的排列顺序讲TMB分为高中低。位于0-25%区间的TMB为高,26%-75%为中,76%-100%为低。 不同公司划分的区间有所区别。
五、 TMB存在的问题
尽管TMB是一个很有前途的生物标记物,但仍有几个问题存在。
- 首先是高TMB的定义或临界值,以及它是否应该取决于肿瘤类型。
- 另一个涉及计算TMB的最佳策略,包括技术实验室方法、要纳入的基因数量或区域、筛选生殖系变异的方法以及其他生物信息学方法。
目前,有几个工作组的目标是提出建议和证据,以使TMB计量法标准化。的确,从病理学家的角度来看,TMB计分的标准化将极大地促进TMB作为常规生物标记物应用于临床实践。最后,TMB作为临床生物标记物的真正有用性仍在临床试验环境中进行评估,还需要更多的数据和证据来支持这种生物标记物在病理学实践中的常规实施。此外,相较于采取有限的、单一的生物标志物,当TMB与PD-L1、T细胞炎症标志物等其他生物标志物联合使用时,TMB可能有其最大的用处。
五、其他信息
TMB是更广谱的免疫治疗biomarker,已从临床研究热点正逐步走向临床应用。TMB越高(TMB-H),肿瘤产生的neoantigen越多,肿瘤免疫原性越强,越适合I-O免疫治疗。CheckMate-026、 CheckMate-227等多项大型临床试验已证实TMB临床应用价值,I-O免疫治疗的ORR(客观缓解率)与TMB呈正相关。束永前教授、宋勇教授都指出TMB越高,临床获益越多,各种肿瘤(肺癌、黑色素瘤、泌尿系统肿瘤等)趋于一致。郭军教授指出,中国的黑色素瘤亚型免疫原性低于国外的患者,原因在于中国亚型的患者TMB值低,而TMB低代表了免疫治疗总体有效率低。
从TMB的定义可以看出,最直接有效的计算TMB的方法就是全外显子测序,然而考虑到实验周期和成本,也有根据靶向热点基因设计的各种panel,该方法成本低,周期快,然而得到的TMB分值没有WES准确。
然而,TMB也有缺陷。周彩存教授指出,TMB的检测远比想象的复杂,基因突变有点突变、插入缺失突变、拷贝数变异等,显然不同种类突变的预测意义是不一样的,插入/缺失突变产生新生抗原的机会可能更大,不同种类突变的权重需要专业的检测公司来评价。例如肾癌的抗PD-1/PD-L1疗效,无法简单通过TMB预测,原因可能是插入/缺失突变导致的neoantigen更多,而实际其TMB的权重可能没有那么高。全外显子检测TMB存在检测周期长,经济成本高等缺点,checkmate026研究用的foundation medicine的大panel(315个基因),结果显示该panel的检测结果与WES的检测结果相关性非常好;MSKCC的大panel(341基因)、裕策生物的大panel(811基因)检测结果与WES相关性也很强。Panel做的足够大设计的又合理,可以取代WES,NGS大panel作为伴随诊断是大趋势。单纯地TMB并不能解决所有的问题,例如对于炎性肿瘤和非炎性肿瘤都有TMB的高表达,但是非炎性肿瘤的免疫治疗效果并不好,况且TMB的cutoff值与PD-L1表达一样,并没有统一标准。宋勇教授指出PD-L1表达与TMB弱相关,即高TMB与高PD-L1表达不是同一人群,我们需要更多Biomarker。
参考资料
- https://mp.weixin.qq.com/s/-vCnGxe8P-iBfQ5_Z_ljNg
- http://blog.sciencenet.cn/blog-2095011-1169414.html
- https://www.seqchina.cn/5560.html
- https://en.wikipedia.org/wiki/Biomarker
- https://baike.baidu.com/item/MSI/9773455?fr=aladdin
- https://www.jianshu.com/p/f67927ece2c5
- https://www.sohu.com/a/382227851_120554400
