【1.3.3.3】B细胞记忆--建立两道防御病原体的墙
There are [pathogens] I’ll remember
All my life, though some have changed
— In My Life, Lennon–McCartney (1965)
幸存一次感染通常会导致对感染病原体的终生免疫。 这种保护在很大程度上是由两个主要的B细胞记忆“壁”(walls)介导的,即长寿浆细胞(plasma cells)和记忆B细胞(memory B cells)。 驱动长寿浆细胞和记忆B细胞产生的细胞和分子过程是深入研究的主题,对全球健康具有重要意义。 确实,尽管当今使用的几乎所有疫苗都取决于其诱导B细胞记忆的能力,但我们尚未成功开发出针对世界上一些最致命的疾病(包括艾滋病和疟疾)的疫苗。 在这里,我们描述了抗原驱动长寿命浆细胞和记忆B细胞生成的两阶段过程,并突出了成功开发每个阶段疫苗的挑战。
一、前言
几个世纪以来,对免疫记忆赋予保护作用的认识先于我们对这种记忆的细胞和分子基础的了解。公元前430年在雅典的一场瘟疫中,公民们了解到,有幸能够从这种疾病中恢复过来,他们可以照料新来的灾民,因为没有人被“袭击两次,至少没有致命”。爱德华·詹纳(Edward Jenner)开发天花疫苗的基础是一种简单的原理,即感染的存活或暴露于低毒力或减毒的病原体会导致终身免疫,这是天花疫苗的基础,天花疫苗是一种能够消灭整个欧洲人口的传染病,在1700年代中期。即使是相当新近的疫苗,例如引起对小儿麻痹症,麻疹和风疹的保护性免疫的疫苗,在很大程度上也没有对免疫基础的机制有全面的了解。不幸的是,并非所有开发疫苗的尝试都是成功的。更糟糕的是,实际上已证明某些疫苗对人类有害,如呼吸道合胞病毒的悲剧性案例。此外,迄今为止,我们还没有成功为世界上一些最致命的疾病(包括艾滋病和疟疾)生产有效的疫苗。希望是,对于形成保护性,长寿命抗体应答和B细胞记忆的细胞和分子机制有更详细的了解,将可以为目前我们尚无的病原体开发安全,有效的疫苗。此外,此类知识可能具有更广泛的益处;例如,对于全身性自身免疫性疾病和B细胞肿瘤的治疗方法的开发,可能部分是驱动产生B细胞记忆的意外结果。
我们现在了解到,许多传染病的免疫记忆是在一次感染后获得的,并且依赖于记忆的两个主要“壁”(wall)的获得。即长寿命的浆细胞,产生保护性抗体和记忆B细胞,能够对病原体及其变体进行再感染。最近几次出色的评论中详细介绍了此过程。在对抗原的主要应答中,来自幼稚B细胞库的抗原驱动的长寿命浆细胞和记忆B细胞的生成主要发生在B细胞滤泡的次级淋巴器官(SLO,secondary lymphoid organs)和连续两个连续的生发中心(GC,germinal centres)中阶段。
- 在阶段1中,通过B细胞抗原受体(BCR)进行的抗原刺激会诱导幼稚B细胞分化为B细胞卵泡中的短暂浆细胞和GC B细胞。
- 在阶段2中,抗原驱动GC B细胞分化为GC中的长寿命浆细胞和记忆B细胞。在随后的对抗原的召回反应中,记忆B细胞通过分化为长寿浆细胞或通过重新进入GC反应来做出反应。
在本综述中,我们描述了记忆B细胞发育的两个主要阶段,重点介绍了预测每个步骤成功的关键变量。我们还简要介绍了包括爱滋病和疟疾在内的慢性传染病如何可能会破坏保护性B细胞记忆的获得。在这种情况下,我们推测了针对此类慢性感染性疾病的疫苗开发的跨越性用途,并通过预防性,广泛中和性抗体提供保护。
二、B细胞记忆的第一阶段 Phase 1 of B cell memory
2.1 抗原驱动的幼稚B细胞分化
原始B细胞首先在SLOs的B细胞卵泡中遇到抗原(图1)。抗原与BCR的结合会导致下游BCR信号传导以及MHC II类分子上BCR结合抗原的内在化,加工和呈递。抗原激活的天然B细胞增加其代谢活性,并表达趋化因子受体(CC趋化因子受体7(CCR7)和EBI2),将其引导至T细胞区的边界,在此处它们与抗原特异性T辅助细胞(TH)相互作用抗原呈递树突状细胞(DC)引发以分化为T滤泡辅助细胞(TFH细胞)的细胞(框1)。最近的研究表明,在病毒感染期间,由产生IL-4的天然杀伤性T细胞介导的滤泡边缘B细胞反应可能还有其他调控层。幼稚的B细胞似乎是多能的,与TH细胞相互作用后至少具有三个命运。幼稚的B细胞可以分化成短寿命的浆细胞,尽管亲和力相对较低,但它们可以迅速产生转换和非转换同种型的病原体特异性抗体。寿命短的浆细胞积聚在淋巴结的脾脏和髓索的红髓区域,其寿命通常受限于感染过程。幼稚的B细胞也可以分化为GC B细胞,随后将在第2期进入GC,并分化为长寿的浆细胞和记忆B细胞。幼稚的B细胞也可能独立于GC产生卵泡中的记忆B细胞。确实,无法发育GC的BCL-6缺陷小鼠中的B细胞已分化为未获得体细胞超突变(SHM)的IgM +和IgG +记忆B细胞,但这些B细胞并未分化为长寿浆细胞。随后的研究表明,主要是IgM阳性的非GC依赖性记忆B细胞在免疫应答的早期直接来源于多能前体细胞,而这些相同的前体在2006年底也产生了GC依赖性,转换的免疫球蛋白阳性记忆B细胞。最后,长寿记忆B细胞以及短寿浆细胞和长寿浆细胞均可通过非GC和T细胞独立机制生成。不依赖T细胞的I型和II型抗原均已显示可产生长寿命的浆细胞。记忆B细胞显示出被非T细胞非依赖性II型多糖抗原诱导。然而,这些记忆B细胞表现出非常低的SHM和同种型转换水平,在表型上不同于幼稚B细胞对T细胞依赖性抗原的反应所产生的记忆B细胞,并且在次级反应中受到免疫特异性IgG抗体的严格调控抗原。重要的是,独立于T细胞的II型多糖疫苗(如Pneumovax)可在成人中提供长期的抗体保护。

在主要反应的第1阶段(左),幼稚B细胞退出循环,进入次要淋巴器官的B细胞滤泡,并调查环境中的抗原。滤泡树突状细胞(FDC,follicular dendritic cells)上遇到的抗原通过B细胞受体(BCR)激活B细胞,抗原被加工并在T细胞-B细胞边界呈递给T细胞,从而驱动幼稚B细胞增殖并分化为三个主要细胞类型:非生发中心(GC)的记忆B细胞,GC B细胞或短寿命浆细胞。在主要反应的第2阶段(右),新分化的GC B细胞形成GC,并在暗区经历增殖和体细胞超突变,然后离开亮区,在那里GC B细胞在FDC上遇到抗原,将抗原呈递给T滤泡辅助细胞(TFH细胞)经历了三个主要命运:即分化为记忆B细胞,分化为长寿浆细胞或重新进入GC暗区。在次要反应中(右下),记忆B细胞对抗原做出反应,并分化为长寿命浆细胞或发生GC反应的GC B细胞。 TCR,T细胞受体。
不同的抗原驱动的T细胞依赖性命运对感染的结果具有深远的影响,导致短期存活的浆细胞提供能够控制初始感染的立即短期存活的抗体反应,或者导致长期存活的GC B细胞 通过分化成长寿浆细胞和依赖于GC的记忆B细胞来维持B生命,尽管经过几天的延迟才能完成GC反应。 我们还没有一个完整答案的一个基本问题是,决定这一命运决定的因素是什么?
B细胞存储器中的TFH细胞 TFH cells in B cell memory
B细胞与CD4 + T辅助细胞的相互作用对于此过程的第1阶段和第2阶段B细胞记忆的发展至关重要。 T卵泡辅助细胞(TFH细胞,T follicular helper cells)是分化的CD4 + T细胞的一个特殊子集,其特征在于转录因子BCL-6的表达。 TFH细胞的分化始于树突状细胞对幼稚T细胞的引发,并涉及随后的引发T细胞与在T细胞区和B细胞滤泡边界的抗原呈递活化的幼稚B细胞的相互作用。这会诱导活化的T细胞(“ TFH前细胞”)进入卵泡并分化为成熟的TFH细胞。 TFH细胞向生发中心B细胞提供关键的辅助信号。其特征是免疫突触中的细胞表面T细胞-B细胞相互作用,主要涉及CD40L-CD40,ICAM1-LFA1和SLAM家族成员,以及TFH细胞分泌的细胞因子IL-4和IL-21。 TFH细胞和B细胞参与相互的信号传导,在反馈回路中发挥作用。生发中心B细胞的命运似乎是B细胞整合B细胞受体信号和TFH细胞帮助信号所致。有关更多详细信息,请读者阅读两篇优秀评论
2.2 前程频率,抗原亲和力和亲和力 Precursory frequency, antigen affinity and avidity
最近的一项研究提供了有关抗原驱动的幼稚B细胞分化过程的重要见解。作者研究了影响表达天然人B细胞的小鼠中疫苗接种结果的因素,这些B细胞表达人种系VRC01类BCR,它们识别HIV gp120的广泛中和表位(参考文献25)。利用可用于确定VRC01 B类细胞的频率和抗原亲和力的大量工具以及对VRC01 B类细胞抗原的详细了解,这项研究提供了证据,表明表达种系VRC01-的幼稚B细胞的前体频率。 BCR类(约1/ 10^6),抗原亲和力(小于1μM)和亲和力(avidity )(抗原表位valency 大于60)相互依赖地限制了GC的成功完成。高亲和力多聚体抗原被证明能够驱动相对稀有的VRC01类幼稚B细胞分化为GC B细胞,该B细胞经过广泛的SHM并在单次免疫后分化为记忆B细胞。
有关GC B细胞分化与浆细胞分化的转录调控的最新研究为抗原亲和力在命运决定中的作用提供了更多证据。转录因子干扰素调节因子4(IRF4),它调节浆细胞的分化,据IRF4的表达水平决定,它也可以启动GC B细胞的生成,IRF4的表达水平取决于BCR信号传导的强度。 IRF4的短暂低水平有利于GC细胞命运,而IRF4的持续较高水平则促进了浆细胞的生成。这些发现表明,导致IRF4弱诱导的低亲和力抗原-BCR相互作用将启动GC B细胞分化,而诱导高水平IRF4的高亲和力抗原-BCR相互作用将促进浆细胞分化。通过CD40L诱导的CD40信号传导和IL-21提供的TFH细胞帮助似乎在指导幼稚B细胞趋向GC分化与浆细胞分化方面发挥了作用。然而,慢性CD40信号传导拮抗GC B细胞的分化并促进浆细胞分化。最近,有证据表明,B细胞命运的决定是通过多步过程做出的,其中CD40信号传导仅在较早时才可实现BCL-6表达的增加,而CD40信号传导的延长则驱使前体远离GC B细胞命运
这些发现提出了一个重要的问题:BCR亲和力对幼稚B细胞命运的影响有多严格?最近的研究比较了BCR诱导的人扁桃体原初B细胞与GC B细胞的BCR诱导活化的亲和力阈值,这提供了证据,表明幼稚B细胞的固有亲和力阈值为GC B细胞的固有亲和力阈值1/100。 在这项研究中,幼稚B细胞表达的BCR对抗原的亲和力估计为〜0.5μm,与先前描述的研究中建议的针对幼稚VRC01-B类B细胞选择的建议最小亲和力阈值(约1μm)[25]。鉴于这些亲和力处于功能性抗体亲和力的最低范围,因此似乎在抗原驱动的分化的第一阶段中,几乎没有亲和力依赖性的抗原特异性幼稚B细胞被排斥。甚至相对低亲和力的抗原特异性幼稚B细胞也会进入GC,并有机会分化为高亲和力的长寿命浆细胞和记忆B细胞。因此,在阶段1中可能很少“浪费”抗原特异性B细胞,因为对抗原的高亲和力不是必需的。
2.3 命运指导的分子机制 Molecular mechanisms of fate instruction
最近的几项研究探讨了指示体内B细胞和体内GC命运的B细胞的分子机制,强调了代谢变化和TFH细胞相互作用的重要性。在一项研究中,含有缺乏蛋白激酶Cβ(PKCβ),B细胞极化和雷帕霉素(mTOR)复合物依赖性代谢重编程机制的关键调节因子的B细胞的小鼠,在用HCV免疫后,无法发育浆细胞或GC。 T细胞依赖性抗原。在此之后,BCR信号在幼稚B细胞中被证明可触发从经典到非经典自噬的转变,非经典途径的增强改变了线粒体的稳态,并影响了GC和浆细胞的命运决定。在另一项研究中,含有B细胞的小鼠与T细胞形成长期结合物的能力减弱,免疫后,它们形成GC和产生亲和力成熟抗体的能力严重受损。在这项研究中,形成B细胞-T细胞偶联物的能力降低是由于intersectin 2(ITSN2)的缺乏,intersectin 2是CDC42的鸟嘌呤交换因子,GTPase是响应BCR的肌动蛋白细胞骨架重塑所必需的发信号。
2.4 抗原结构的影响 Impact of antigen structure
抗原的性质和结构也影响免疫结果。特别令人关注的是与细菌膜复合物(如脑膜炎奈瑟氏球菌的外膜复合物)或病毒样颗粒偶联的弱免疫原性重组亚基抗原的复合物,它们是由病毒结构蛋白组成的非复制性壳,当过表达时会组装成密集的多蛋白阵列。这些抗原被证明具有极高的免疫原性,并能够常规诱导高滴度持续性抗体应答,尽管对其效力的潜在机制尚不十分了解。确实,非常成功的人乳头瘤病毒(HPV)疫苗包含由四种HPV类型的主要L1蛋白组装而成的病毒样颗粒,可为幼稚个体提供近乎完全的保护,使其免受性传播的HPV感染,甚至可能在接种时有效。已显示,HPV疫苗可在初次接种疫苗的个体中诱导记忆B细胞,这些个体表达有效的中和抗体,但未经历过广泛的SHM免疫。
抗原的另一个重要特征是它们在体内呈递的形式。抗原通过囊下鼻窦通过传入淋巴管到达SLO。表达LYVE1的淋巴样内皮细胞和周围表达CD169的巨噬细胞的网络形成了紧密的屏障,可阻止大抗原和抗原复合物进入B细胞滤泡。然而,已经证明,小抗原,如鸡蛋清溶菌酶(HEL; 14.4 kDa)在注射后数分钟内即可穿透B细胞卵泡,并进入囊下窦或淋巴管的孔中。较大的抗原(超过70 kDa),病毒和病毒样颗粒被荚膜下窦巨噬细胞以免疫复合物或补体偶联复合物的形式捕获。它们迅速穿梭到非同源B细胞中,这些B细胞将抗原转运到卵泡中,复合物沉积在卵泡DC(FDC)上,在B细胞反应期间连续提供抗原。 FDC还提供3D网络,B细胞在该网络上在卵泡内移动并分泌CXC-趋化因子配体13(CXCL13),后者在GCs中募集并保留表达CXC-趋化因子受体5(CXCR5)的B细胞。在SLO中,B细胞同时暴露于可溶性和FDC相关抗原的事实提出了一个重要问题:B细胞暴露于可溶性抗原与膜相关抗原的结果是否相似?众所周知,膜相关抗原在触发B细胞活化方面非常有效。此外,一些体外研究提供了证据,证明B细胞对可溶性抗原的反应要求与膜相关抗原的要求在许多参数上有所不同,包括对共受体的要求,对单价抗原的响应,细胞骨架的调节和BCR团簇的动力学和调控。然而,目前我们几乎没有关于在体外或体内对可溶性抗原和膜相关抗原作出反应的B细胞命运的信息。疫苗设计似乎将从这些信息中受益。
2.5 病原体产物在微环境中的作用 Effect of pathogen products in the microenvironment
B细胞滤泡内的微环境对未成熟B细胞命运的影响才刚刚开始探索。一个重要的环境因素是病原体或病原体产品的存在,以及它们通过先天免疫受体发送给宿主的危险信号。最近的一项研究表明,病原体相关的分子模式(PAMP),特别是Toll样受体9(TLR9)的CpG配体,对幼稚B细胞产生了意想不到的作用,即在抗原内化后的某个时刻阻止了抗原的加工和呈递,但在将抗原递送至处理室之前。因此,CpG刺激的B细胞获得T细胞帮助的能力较弱。平行研究提供了证据,表明由于诱导的线粒体功能异常(“代谢时钟”),BCR信号传导后不久就无法获得T细胞的活化B细胞有所帮助。这些研究还表明,TLR9刺激使抗原激活的B细胞免于凋亡,并使其增殖和分化成低亲和力的短寿命浆细胞。综上所述,这些观察结果提供了一种机制,通过该机制,病原体产物存在时激活的幼稚B细胞注定会迅速分化成短寿命的浆细胞,而不是参与费时的GC反应(图2)。
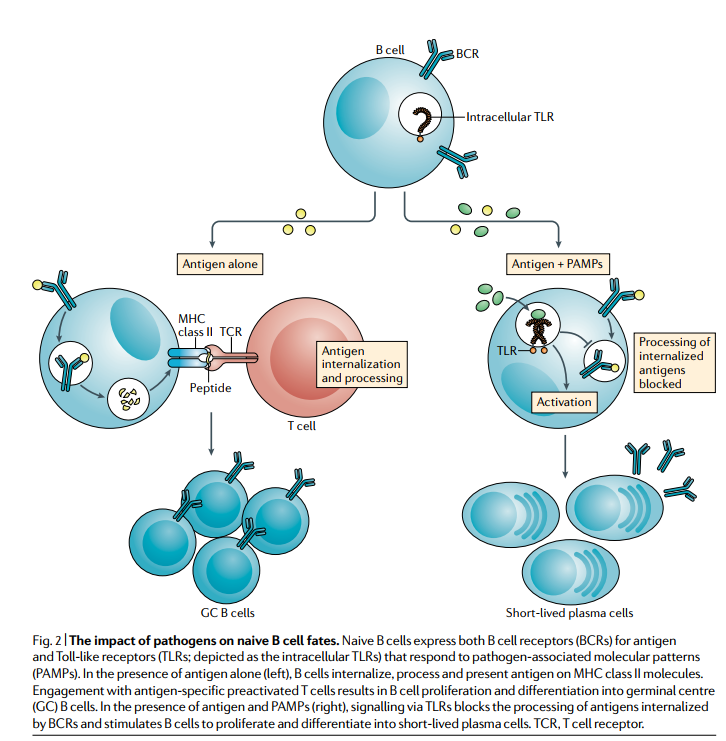
幼稚的B细胞既表达抗原的B细胞受体(BCR),又表达对病原体相关分子模式(PAMP,pathogen-associated molecular patterns)响应的Toll样受体(TLR;描绘为细胞内TLR)。 在单独存在抗原的情况下(左),B细胞在MHC II类分子上内化,加工并呈递抗原。 与抗原特异性预活化T细胞的结合导致B细胞增殖并分化为生发中心(GC)B细胞。 在存在抗原和PAMP的情况下(右),通过TLR发出的信号会阻断BCR内在化的抗原的加工,并刺激B细胞增殖并分化为短寿命的浆细胞。 TCR,T细胞受体。
CpG对B细胞对T细胞依赖性抗原的拮抗作用的发现令人惊讶,因为众所周知,对T细胞依赖性抗原的免疫应答需要佐剂,其中许多都含有PAMPs作为免疫刺激成分。常规的DC通过在到达SLO激活T细胞之前增加其抗原呈递细胞的功能来增强抗原呈递细胞的功能,从而对周围组织中遇到抗原的PAMP作出反应,这是佐剂的明显好处。的确,黄热病疫苗YF-17D是有史以来最成功的经验性疫苗之一,它通过多个TLR激活DC。但是,刚刚描述的研究表明,如果PAMP积聚在B细胞卵泡中,B细胞将立即分化为相对低亲和力的短暂浆细胞,从而对即将发生的危险信号做出反应。该研究表明,以CpG作为佐剂用蛋白抗原免疫小鼠和人类会导致高水平的无法亲和力成熟的抗体,这与GC非依赖性浆细胞的产生是一致的。这些观察结果表明,对于需要高SHM水平的病原体特异性反应(例如广泛中和HIV特异性抗体反应),PAMPs或CpG可能不是理想的佐剂。
是否有更好的佐剂制剂来驱动幼稚B细胞分化为可在GC中积累SHM的GC B细胞?在非人类灵长类动物模型中,对八种常用佐剂对HIV包膜蛋白的抗体反应的影响的最新比较表明,与佐剂一起配制包膜蛋白可增加HIV特异性抗体的水平,但不会增加广泛中和抗体的发展所必需的SHM的频率。因此,未来对佐剂功效的评估可能不仅需要评估抗体滴度和反应持续时间,还需要评估刺激GC反应导致SHM和亲和力成熟的证据。
二、B细胞记忆的第二阶段 Phase 2 of B cell memory
2.1 抗原驱动的GC B细胞分化
与记忆产生的第一阶段相反,如前所述,抗原亲和力选择似乎在命运决定中起着最小的作用,发生在GC中的记忆产生的第二阶段主要是通过产生高亲和力B细胞选择(图1)。在这个阶段,从幼稚B细胞分化而来的GC B细胞进入新形成的GC,它们是紧密排列在卵泡内的细胞簇。在这里,GC B细胞高度表达转录因子BCL-6和G蛋白偶联受体鞘氨醇1-磷酸受体2(S1P2),从而促进它们在GC中的保留。在GC暗区中,GC B细胞增殖并经历SHM,然后退出进入GC亮区,在那里它们被选择经历三种命运之一。首先,一些GC B细胞分化成长寿浆细胞,这些浆细胞在骨髓中停留并主动分泌大量抗体,在没有抗原或没有第二次攻击的情况下可以持续数年,甚至是一生,。其次,一些GC B细胞分化为长寿命记忆B细胞,它们是静止的细胞,位于SLO和其他组织中促进其暴露于抗原的壁中。第三,GC B细胞可能会重新进入GC暗区,以进行其他轮次SHM和选择,最终产生记忆B细胞或长寿浆细胞。在二次反应中,在抗原攻击后,记忆B细胞被激活并具有至少两个命运:它们要么分化成长寿浆细胞,要么进入GC进行几轮种群扩展,SHM和选择(图1)。
2.2 亲和力阈值和GC B细胞选择 Affinity thresholds and GC B cell selection
要了解GC中的亲和力选择,B细胞感知其对抗原的亲和力的机制至关重要。如前所述,GC中可能同时存在可溶性抗原和膜相关抗原。目前,对B细胞感觉其对可溶性抗原亲和力的机制了解甚少。相比之下,B细胞结合抗原,响应抗原并使其内在化以进行加工和呈递的能力被证明直接取决于B细胞对抗原的亲和力。 B细胞通过对BCR抗原复合物施加拉力来从膜中捕获抗原。较高亲和力的相互作用更能抵抗拉力,并且在内化抗原以呈递给TFH细胞方面更成功。因此,B细胞亲和力是由B细胞能够从FDC捕获并在GC中呈现给TFH细胞的抗原量间接决定的(图3)。
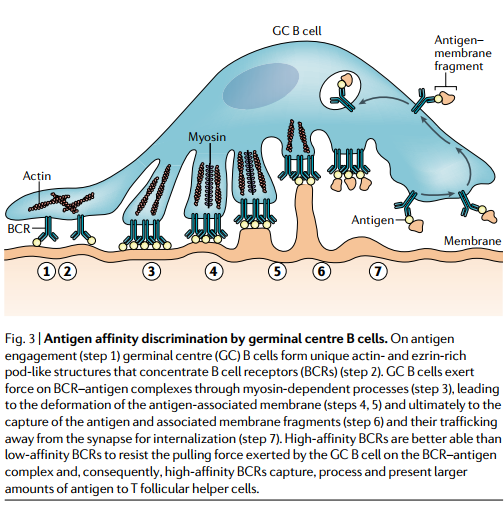
通过抗原结合(步骤1),生发中心(GC)B细胞形成独特的富含肌动蛋白和ezrin的豆荚状结构,从而浓缩B细胞受体(BCR)(步骤2)。 GC B细胞通过肌球蛋白依赖性过程(步骤3)对BCR抗原复合物施加作用力,导致抗原相关膜变形(步骤4、5),并最终导致抗原和相关膜片段的捕获(步骤 6)以及将其贩运远离突触进行内部化(第7步)。 高亲和力的BCR比低亲和力的BCR更能抵抗GC B细胞对BCR抗原复合物施加的拉力,因此,高亲和力的BCR可以捕获,加工并向T滤泡辅助细胞呈递大量抗原 细胞。
如果亲和力选择在GC反应中至关重要,GC B细胞是否特别适合区分抗原亲和力并由高亲和力抗原选择?如前所述,最近的研究提供了证据,表明GC B细胞对BCR信号传导和抗原内在化的固有亲和力阈值比幼稚B细胞至少高100倍。最近的研究还提供了证据,表明GC B细胞具有“重新连接”的CD40和BCR信号转导,使得CD40信号通过核factor-κB进行转导,而BCR信号通过叉头盒蛋白O1(FOXO1)进行转导,并且这两个信号通路都是必需的诱导MYC,这对于GC B细胞存活至关重要。相反,幼稚的B细胞可以单独通过BCR或CD40发出信号来激活MYC。这种重新布线的最终结果是,与原始B细胞相比,GC B细胞对抗原和T细胞的激活要求更高。
此外,GC和原始B细胞在细胞表面受体的表达上有所不同,这可能有助于进一步提高GC B细胞的亲和力阈值。例如,与未加工的人类B细胞相比,人类GC B细胞表达的VLA4(也称为α4整联蛋白)非常少,这是一种整联蛋白,通过与VCAM1结合来稳定与抗原携带DC的初始相互作用,从而降低了亲和力阈值用于B细胞活化。此外,与幼稚B细胞相比,GC B细胞在小鼠中显示可通过专门的免疫突触结构识别抗原。随后的研究提供了GC B细胞结构的详细图片,表明GC B细胞表达的BCR集中在独特的,高度动态的含肌动蛋白和ezrin的豆荚状结构中,BCR通过这些结构施加拉力和测试亲和力。值得注意的是,GC B细胞与抗原的亲和力决定了豆荚状结构的行为。低亲和力抗原诱导抗原结合和释放的动态搜索行为,而高亲和力抗原诱导GC B细胞与含抗原膜的稳定长寿命结合。对这些GC B细胞荚状结构中BCR信号启动的潜在机制的更详细的了解可能会为深入了解疫苗设计提供信息,以最大程度地选择高亲和力的GC B细胞。
2.3 GC B细胞的进一步分化
我们刚刚开始获得答案的一个核心问题是,如何控制GC B细胞相对于GC中的记忆B细胞分化为长寿浆细胞。目前,数据支持在驱动浆细胞分化与记忆B细胞分化的GC过程之间进行基本二分法的概念。使用5-溴脱氧尿嘧啶核苷脉冲标记的研究提供了证据,表明GC响应在成熟时会经历时间转换,首先产生具有有限SHM的记忆B细胞,然后产生包含更高度变异的可变(V)基因的长寿浆细胞。在记忆B细胞区室中观察到的突变很少,这表明与长寿命浆细胞的突变率更高的BCR相比,B细胞的亲和力选择水平更低,并且具有更广泛的交叉反应性BCR。最近的研究直接表明,亲和力选择不能平等地应用于记忆B细胞和长寿浆细胞的前体,从而导致高度选择的高亲和力长寿浆细胞和广泛反应性的较低亲和力记忆B细胞。对单个硝基苯基特异性浆细胞和记忆B细胞的分析提供了证据,表明严格选择高亲和力浆细胞是GC响应免疫接种的初始输出。相反,只有65%的记忆B细胞能够产生高亲和力的抗体,表明选择的严格度较低。与这些观察结果一致,其他研究表明,只有通过SHM获得高亲和力BCR免疫抗原HEL的GC B细胞才能分化为浆细胞。随后的研究提供了有关将GC B细胞选择入浆细胞谱系的更多机制细节,表明表达转录因子IRF4的BCL-6lowCD69hi GC B细胞对浆细胞谱系的承诺有所帮助(参考文献66)。 BCL-6lowCD69hi GC B细胞的表达也表达高水平的ICAM1和SLAM,受CD40介导的T细胞介导的信号传导的调控,这表明TFH细胞与GC B细胞的相互作用是产生GC B细胞的关键。易于分化为长寿命浆细胞。
研究表明,CCR6在GC轻区中唯一标记了记忆B细胞前体,并且这些记忆B细胞前体主要表达低亲和力的HEL特异性BCR67,从而提供了有关记忆B细胞分化的其他详细信息。使用转基因小鼠模型的研究表明,GC B细胞具有可诱导性标记,亲和力较低的BCR轻区B细胞更易于进入记忆B细胞池68。这些易于记忆的B细胞B细胞表达较高水平的转录阻遏物BACH2,其BACH2表达水平与T细胞提供的帮助强度成反比。这些数据支持了一个指导性模型,用于选择记忆B细胞,其中T细胞决定BACH2表达,从而促进向记忆B细胞的分化,也许是通过通过BACH2的抗增殖或存活功能促进记忆B细胞向静止的过渡(参考。 68)。
由于记忆B细胞通过分化为浆细胞或GC B细胞而提供了第二级保护,以防止再次暴露于病原体,因此最近的研究集中于确定两种命运是否都存在于所有记忆B细胞中。使用标记了表达激活诱导的胞苷脱氨酶(AID)的B细胞的小鼠模型进行的研究表明,它们参与了GC反应,结果表明,用绵羊红细胞(一种颗粒抗原)进行免疫可以产生多种具有不同功能的记忆B细胞亚群。这些包括在GC样结构中持续了几个月的IgM +和IgG + B细胞,以及在卵泡外积累的IgM +和IgG +记忆B细胞。在抗原攻击后,与分化为浆细胞的IgG +记忆B细胞相反,IgM +记忆B细胞进入了GC。在转基因小鼠模型中,显示IgG1 +记忆B细胞易于分化为浆细胞,并且是次级反应中IgG1抗原特异性抗体的主要来源。
免疫后在另一项研究中追踪了在C57BL / 6小鼠中表达IgM(IgM +)或同种型转换的免疫球蛋白(swIg +)的抗原特异性B细胞的命运,发现同时生成了IgM +和swIg +记忆B细胞。但是,在随后的挑战中,尽管IgM +记忆B细胞比swIg +记忆B细胞数量更多且寿命更长,但是swIg +记忆B细胞主导了挑战反应,产生浆细胞和新的记忆B细胞,但没有GC B细胞。随着抗原特异性血清免疫球蛋白水平的下降,swIg +记忆B细胞的数量下降,但是包含少量SHM但具有产生GC B细胞能力的IgM +记忆B细胞持续存在,并成为持久记忆的库。但是,同一组作者的后续研究提出了在C57BL / 6小鼠中swIg +记忆B细胞不稳定和大量IgM记忆B细胞生成的另一种机制,即C57BL / 6小鼠的反应是由异常的单个重链可变域(VH)所控制,该可变域赋予抗原高亲和力。
另一项研究提供了功能独立的记忆B细胞亚群的证据,这些亚细胞基于CD80和PDL2的表达而独立于isotype。面临挑战时,亲和力相对较高的CD80 + PDL2 +记忆B细胞分化为浆细胞,而GC B细胞则没有,相反,亲和力较低的CD80-PDL2-记忆B细胞分化为极少的浆细胞,但能强劲地分化为GC B细胞。 。在另一项研究中,显示CD80hi记忆B细胞是在初次免疫反应期间由高亲和力B细胞产生的,其机制依赖于TFH细胞诱导强CD40信号传导,而发育CD80low B细胞则不需要强CD40信号。
综上所述,这些研究提供了有力的证据,表明记忆B细胞相对于GC B细胞分化为浆细胞的能力可能被划分为几个亚群。为了在疫苗设计中利用记忆B细胞功能的这种区隔,将有必要进一步阐明驱动这些记忆B细胞亚群分化的机制。
2.4 长寿浆细胞和记忆B细胞在保护性免疫中的作用
B细胞记忆的当前模型表明,由长寿浆细胞产生的高度选择的高亲和力抗体形成了抵抗同源攻击的第一道防线,而记忆B细胞则提供了第二层防御变体病原体的防御 逃避了长期存在的浆细胞介导的防御作用(图4)。 记忆B细胞以这种方式起作用的证据有多强?记忆B细胞提供此功能的能力是否取决于累积其他SHM?
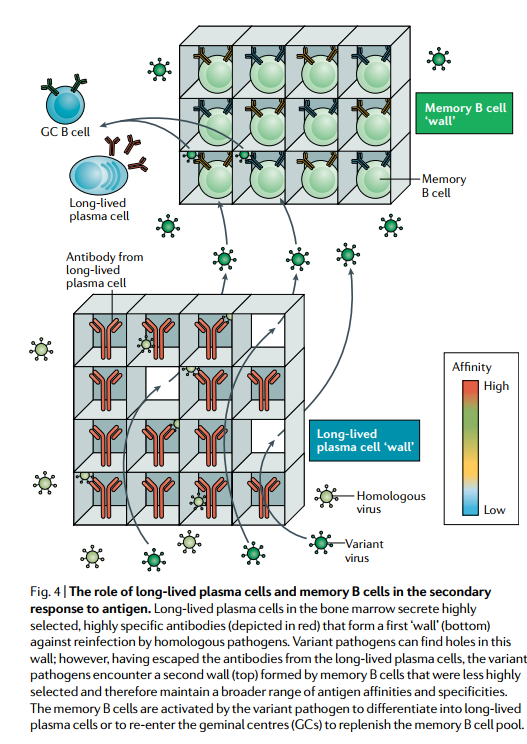
骨髓中的长寿命浆细胞分泌高度选择的高特异性抗体(以红色显示),形成第一道“壁”(底部)以抵抗同源病原体的再感染。 多种病原体可以在此壁上发现孔; 然而,从长期存在的浆细胞中逃脱了抗体之后,变异病原体遇到了由记忆B细胞形成的第二个壁(顶部),该壁的选择性较低,因此可以保持更大范围的抗原亲和力和特异性。 记忆B细胞被变体病原体激活,以分化成长寿浆细胞或重新进入双子中心(GC)以补充记忆B细胞池。
使用西尼罗河病毒感染小鼠模型进行的野生型和变异型病毒感染的研究表明,长效浆细胞产生的抗体仅对野生型病毒产生反应,而野生型和变异型病毒在显着的中和表位中只有一个氨基酸不同中和变异病毒的效果很差。然而,源自记忆B细胞的浆细胞产生的抗体可同等地或显着地识别野生型病毒和变体病毒,并且比野生型病毒更好地识别变体病毒,并且在不积累其他SHM的情况下如此识别。与这些结果一致,研究发现,在先用成田病毒株免疫的小鼠中追踪流感病毒血凝素(HA)特异性B细胞,然后用同源病毒或异源PR8病毒株攻击,证明长期存在的抗体已经分泌了预先存在的抗体。活的浆细胞被保护免受同源攻击,而保护免受异源攻击则需要记忆B细胞激活。这些记忆B细胞主要针对相对不变的HA干。对人类对2009 H1N1大流行性流感疫苗进行疫苗接种的抗体反应的研究表明,针对该疫苗的现有抗体水平较低的个体会产生针对HA茎的广泛反应性抗体,而针对该HA抗体的现有抗体水平较高的个体该疫苗与菌株特异性HA头反应相关,这表明针对HA头的抗体阻止了广泛保护性茎特异性抗体的产生77。因此,一个人的流感病毒免疫史会影响在攻击时产生广泛保护性B细胞反应的能力。
有趣的是,在小鼠中发现,在用H3N2亚型流感病毒免疫期间给予mTOR抑制剂雷帕霉素可减少GC的形成并抑制B细胞的类别转换,但可产生独特的抗体库,可防止异亚型致死性感染H5N1病毒。对用登革热病毒包膜蛋白免疫并用相同或变异病毒蛋白攻击的小鼠的抗体反应的研究表明,变异蛋白主要刺激具有最多样且变异最少的V基因的IgM +记忆B细胞。综上所述,这些研究为高度多样化的记忆B细胞群在提供针对变体病毒感染的广泛保护中的作用提供了有力的证据。未来的挑战将是确定如何差异唤起这些记忆B细胞群体。
四、慢性感染对记忆B细胞的影响
迄今为止,在本综述中几乎所有描述的研究都在急性感染或疫苗接种后挑战的模型中研究了B细胞记忆的产生和功能。这些研究的发现与抗体介导的疫苗的开发最相关,该疫苗可以在幼稚的个体中诱导保护性免疫。但是,迫切需要针对患有慢性感染(包括艾滋病,疟疾和肝炎病毒感染)的个人的疫苗。这种疫苗的开发可能具有很高的挑战性,因为目前的证据表明,这种慢性感染对记忆B细胞区隔有深远的影响,我们刚刚开始理解其影响。例如,慢性感染的一个共同特征是称为“非典型记忆B细胞”的新型T-bet +记忆B细胞群体的大规模扩张。我们尚不了解这些记忆B细胞在人类中的功能,并且尚不完全清楚随着年龄增长和在某些感染中出现的T-bet +记忆B细胞的小鼠模型是否与人类非典型记忆B细胞有关,并且是否可以用作研究非典型记忆B细胞80的模型。因此,我们距离设计用于慢性感染的疫苗可能还有一段距离。
五、预防性抗体
尽管接种疫苗以诱导B细胞记忆是预防传染病的最有效和低成本方法,但事实证明,针对世界上许多最致命的病原体,包括引起艾滋病和疟疾的病原体,开发有效的疫苗具有极大的挑战性和挑战性。迄今为止,收效甚微。未能针对这两种疾病以及其他几种疾病开发疫苗的努力导致人们试图完全跳过疫苗开发,并直接提供高效,广泛中和的抗体作为预防剂(参见参考文献4、5)。这不是一个新主意,因为被动转移抗体已被用作白喉和破伤风等传染病的治疗方法,并随后用于多种病毒性疾病,包括呼吸道合胞病毒,乙型肝炎病毒和丙型肝炎病毒的感染。然而,新的方法是成功成功地生成了针对几种病毒(包括HIV)以及引起疟疾的寄生虫的罕见,高效且广泛交叉反应的人单克隆抗体。另外,抗体工程可以增加此类抗体的效力,交叉反应性和半衰期。这些稀有人类抗体发现的关键是精心选择具有理想血清抗体谱的供体,以及高通量人类B细胞分离技术的发展。目前,预防被动抗体似乎是HIV感染疫苗接种的有前途的替代方法。此外,在小鼠和猕猴中通过载体介导的抗体转移的最新成功(其中单次注射提供了连续和持续的抗体递送)可以提供抗体预防的另一种形式。许多抗病毒和抗疟疾单克隆抗体正在临床开发中,在接下来的几年中这些研究的结果将证明这种方法的当前前景是否得以实现。
六、总结
我们在向公元前430年的瘟疫幸存者提供援助方面走了很长的路要走。雅典解释了自己的运气,永远不会“遭受两次攻击”。我们现在对B细胞记忆的细胞基础(即长寿浆细胞和记忆B细胞)以及这些细胞如何在两个连续的抗原驱动过程中从幼稚B细胞发育中有了很好的了解。我们还对如何构建两个B细胞记忆壁以及如何抵御它们提供的入侵病原体有一个总体概念。我们所知甚少的是如何有效设计疫苗和佐剂,以可再现地产生B细胞记忆。目前,目前尚不清楚一般指导方针是否会从当前研究中得出,或者疫苗设计是否基本上将继续是一个经验过程。鉴于最近人们对B细胞记忆的了解迅速发展,我们感到乐观的是,不久的将来,不久的进步将为开发迫切需要的疫苗以抵御人类最严重的敌人提供新的处方。
参考资料
- Nature Reviews Immunology volume 20, pages229–238(2020). B cell memory: building two walls of protection against pathogens. https://www.nature.com/articles/s41577-019-0244-2?proof=t
