【1.7.2.1】CD20
一、从CD20和CD3看抗体药物研发历程
早在19世纪中叶,人们发现在某些疾病感染者血清中存在能够治疗相关疾病的“杀菌素”,成为了人们对于抗体的初步认知。而从“杀菌素”到抗体的模型的提出,又经历了近一个世纪。说到真正的治疗性抗体药物的研发,则要追溯到上个世纪70年代,Milstein和Kohler尝试将能够产生抗体的B细胞与肿瘤细胞进行了融合,制备出了既能够分泌抗体,又能够无限增殖的杂交瘤细胞。这项技术,对于治疗性抗体药物的研发具有里程碑的意义,Milstein和Kohler也因此获得1984年的诺贝尔生理学或医学奖。
在杂交瘤技术获得诺贝尔奖的第二年,首个治疗用抗体药物Orthoclone OKT3获得了美国FDA的批准,这是一个靶向CD3的抗体,被用于防止肾脏移植后的排异反应。Orthoclone OKT3作为第一个获批的治疗用抗体药物具有划时代的意义,然而,由于其序列来源为鼠源,使得在给药过程中被人体免疫系统当作外源蛋白识别并清除,使得多次给药后的治疗效果下降明显,甚至可能诱发严重的机体免疫相关副反应,甚至致死。这些不良事件的出现给治疗用抗体药物的研发蒙上了一层阴影。
在此基础上,将来自于鼠源的可变区与人源的恒定区进行嵌合,制备出既能够识别靶点蛋白,又降低鼠源序列占比的嵌合抗体,初步降低了异源序列导致的排斥反应。嵌合抗体中的代表作,是罗氏于1997年获批的靶向CD20的用于治疗B细胞淋巴瘤的Rituxan单抗。
伴随着抗体药物研发的不断进展,后续通过抗体人源化改造获得的人源化抗体,以及通过转基因动物或噬菌体/酵母展示技术获得的全人源抗体相关技术路线逐渐成熟,使得抗体药物研发呈现出爆炸式的飞跃。
二、靶向CD20的抗体药物进程
作为B细胞表面抗原,CD20表达开始的稍晚一些,丢失的稍早一些,在前B细胞到成熟B细胞阶段均有表达,而不表达在祖B细胞以及成熟的浆细胞上。CD20同时表达于B细胞来源的淋巴瘤、白血病等肿瘤细胞,涉及炎症和免疫相关疾病的B细胞,因而CD20也成为了淋巴瘤、白血病和某些自身免疫疾病的治疗靶标。
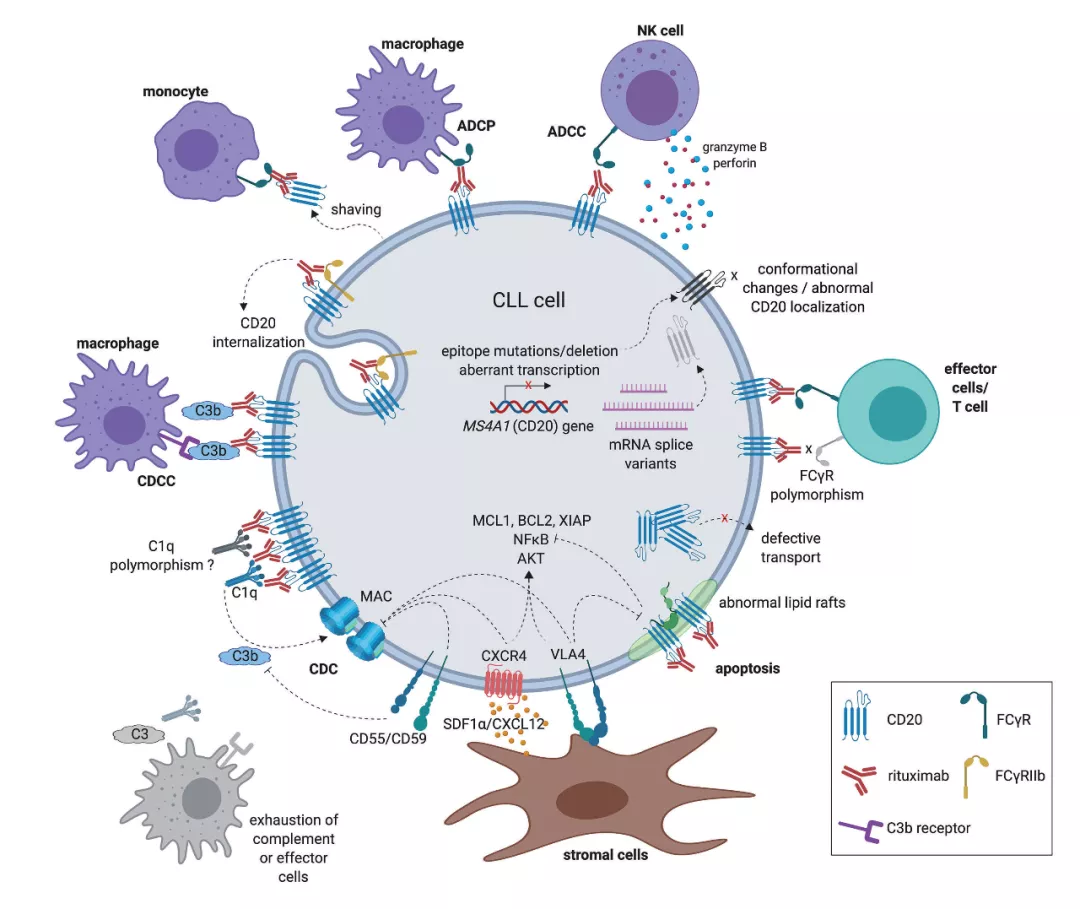
抗CD20抗体的作用机制
靶向CD20的抗体药物经历了三代创新:第一代是以Rituximab(利妥昔单抗)为代表的人鼠嵌合抗体,人源化程度不高,部分患者会产生耐药或者不良反应;第二代是以Ofatumumab(奥法木单抗)为代表的人源化改造抗体,虽然降低了免疫原性,减少了不良反应,但抗体特异性和抗原结合的亲和力有一定的下降;第三代是以Obinutuzumab(奥妥珠单抗)为代表的Fc片段糖基化修饰抗体,增强抗体的特异性及与抗原结合的亲和力,使得ADCC与ADCP效应增强。但临床数据表明,尽管抗CD20单抗已经发展到了第三代,利妥昔的领先地位并没有被撼动。
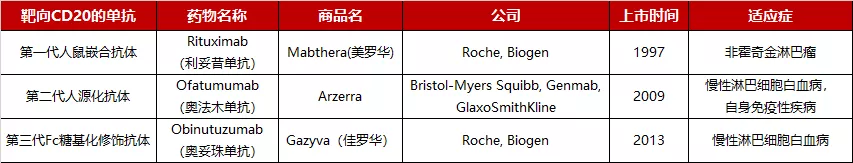
靶向CD20单抗药物开发进展
不局限于单抗药物领域,CD20通过结合CD3等靶点进行双特异抗体的开发实现了将T细胞募集到B细胞周围,进而实现T细胞对于B细胞的杀伤作用。 目前在CD20XCD3的双抗研发领域中,丹麦公司Genmab开发的Epcoritamab(GEN3013)是一种皮下注射的双特异性抗体,目前正在研究用于治疗B细胞非霍奇金淋巴瘤。罗氏布局了两种同时靶向CD20/CD3的不同结构形式的双特异性抗体:Mosunetuzumab和Glofitamab。2020年的美国血液制品年会上,罗氏披露了该药物的临床实验结果:在接受Mosunetuzumab联合CHOP治疗复发/难治性非霍奇金淋巴瘤的患者中总体有效率达到了86%,其中71%的患者达到了完全缓解。目前Mosunetuzumab的相关临床研究覆盖了诸如弥漫性大B细胞淋巴瘤、非霍奇金淋巴瘤、滤泡性淋巴瘤等多个适应症。
Glofitamab则是罗氏开发的一种特殊结构的双特异抗体,含有两个可以结合CD20的结构域以及一个结合CD3的结构域。
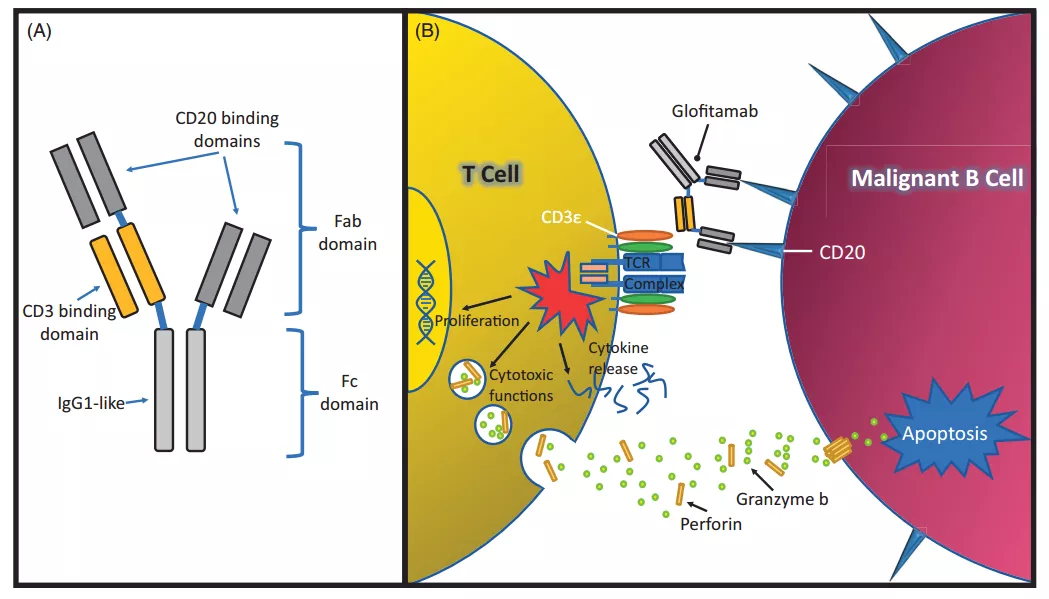
Glofitamab的结构和作用机理
2019年的美国血液制品年会上,罗氏就公布了Glofitamab联合第三代CD20单抗——奥妥珠治疗复发/难治性非霍奇金淋巴瘤的临床试验进展数据:联合治疗的客观缓解率(ORR)为54% (n=15/28),完全缓解率(CR)为46% (n=13/28)。
三、全长CD20蛋白
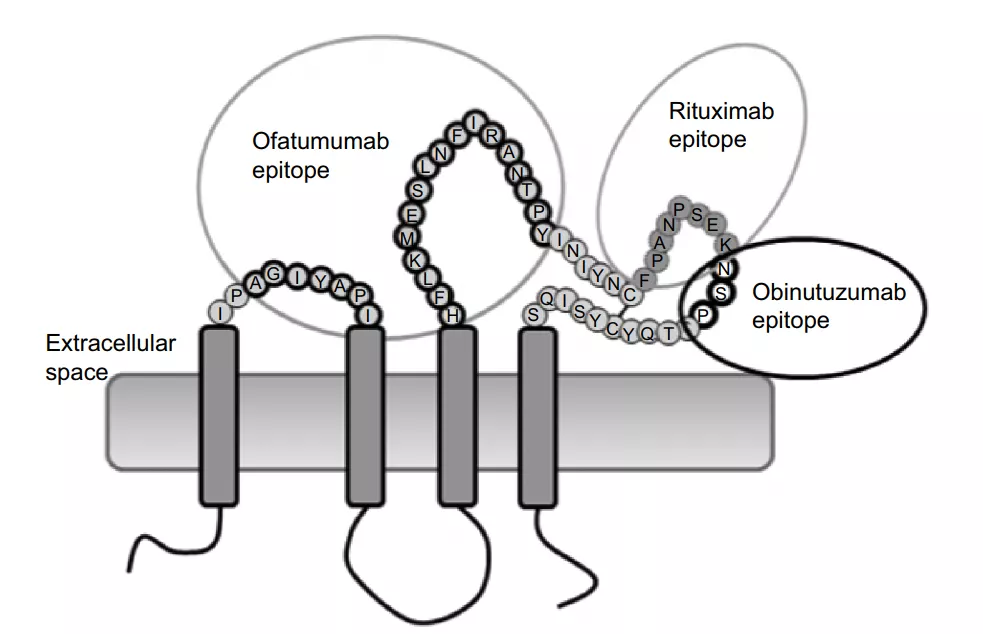
- 具有完整的天然正确构象和完整表位(Rituximab和Obinutuzumab的识别表位是CD20细胞外结构域的一个large loop,Ofatumumab在large loop和short loop均有结合);
- 包括未进行标记的和生物素标记的Nanodisc、DDM/CHS及VLP不同版本产品;
- 可用于免疫/ ELISA/ SPR/ BLI/ FACS;
- 生物活性经Rituximab、Ofatumumab结合验证,展现出纳摩尔级别的高亲和力。
四、靶点机制
CD20 抗原是一种非糖基化磷蛋白,分子量约为 33kD,表达在人的正常 B 细胞和恶 性肿瘤 B 细胞表面,在 B 细胞活化和分化中起关键作用。以 CD20 为靶点的抗体药物可 分为三代:第一代的利妥昔单抗、第二代的奥法木单抗(人源化)及第三代的奥妥珠单抗 (Fc片段经过糖基化修饰),治疗领域不仅有B细胞淋巴瘤,还包括多发性硬化症和免疫 性血小板减少症等。抗 CD20 单抗杀伤 B 细胞肿瘤主要与 3 种作用机制有关,分别是抗 体依赖的细胞毒作用(antibody dependent cell mediated cytotoxicity,ADCC)、补体依赖的 细胞毒作用(complement dependent cytotoxicity,CDC)及抗体与CD20受体结合引起的 直接效应,包括抑制细胞生长、改变细胞周期及促进细胞凋亡。
过去 20 年,以利妥昔单抗(Rituximab)及以它为基础的方案一直是 B 细胞淋巴瘤患 者一线治疗的首选,为患者带来了显著的生存获益。2021 年 6 月,奥妥珠单抗 (Obinutuzumab)作为全球首个经糖基化改造的II型人源化抗 CD20 单克隆抗体,已获得中国药监部门的正式批准,与化疗联合用于初治广泛期滤泡性淋巴瘤,以及缓解患者随后 的单药维持治疗。目前有十几家药企正在研发抗 CD20 单抗,基本都是利妥昔单抗的生物 类似物。国产抗 CD20 单抗的上市不仅可以打破进口产品的垄断局面,预期也会因为其价 格优势,逐渐提升抗 CD20 治疗的覆盖率。

资料来源:Pavlasova G, Mraz M.The regulation and function of CD20: an “enigma” of B-cell biology and targeted therapy[J]. Haematologica, 2020, 105(6): 1494-1506. doi:10.3324/haematol. 2019. 243543. PMID:32482755; PMCID: PMC7271567.
2. 临床研究申报概况
2022年,在中国申请的抗CD20抗体研究一共有8项,其中国际多中心研究有3项; 大部分为I/II期研究,只有 1 项临床研究进入III期阶段。在这 8 项研究中,C-CAR039 是 一种新型的CD19/CD20双靶点CAR-T细胞治疗,正在进行治疗CD19或CD20阳性的复 发/难治性大 B 细胞淋巴瘤的Ib/II期临床研究;HXYT-001 是采用人源化抗体靶向 CD19 和 CD20 的合成性 T 细胞受体和抗原受体(STAR)修饰的 T 细胞创新药物,目前 HXYT- 001 治疗复发/难治性 B 细胞非霍奇金淋巴瘤(B-NHL)的I期临床研究也正在国内进行。 剩余的 6 项研究均集中在同时结合 CD3 的双特异性抗体领域。其中皮下注射剂型的双特 异性抗体 Epcoritamab 有 3 项研究,包括 1 项在复发/难治性弥漫大 B 细胞淋巴瘤患者中 对比 Epcoritamab 和研究者选择的化疗的III期研究;2 项评价 Epcoritamab 单药或与标准 治疗联用治疗 B-NHL 中国受试者的安全性和初步疗效的Ib/II期研究。2022 年 11 月, FDA 已经授予了 Epcoritamab 用于经二线或 2 级以上系统治疗后的复发/难治性大 B 细胞 淋巴瘤患者优先审评资格。另外 3 项 CD20/CD3 双特异性抗体的研究分别为 JS203 在 B- NHL 患者中的国内I期临床研究,GB261 治疗 B-NHL 和慢性淋巴细胞白血病的国际多 中心I/II期研究,以及在复发/难治性滤泡性淋巴瘤患者中进行的 1 项Ib/II期国际多中 心研究,该研究分为 2 个阶段,非随机化阶段是评价 Mosunetuzumab 加来那度胺(+ LEN) 或 Glofitamab+LEN 伴或不伴奥妥珠单抗给药的安全性、药代动力学和有效性,随机化阶 段是比较皮下注射对比静脉注射 Mosunetuzumab+LEN 的疗效和安全性。2022 年 12 月, FDA 已经批准 Mosunetuzumab 用于接受过二 线或二线以上全身治疗后 R/R FL 成人患者 的治疗。
3. 简评
目前,我国多家医药企业正在积极研发抗 CD20 单抗,也已经有多个抗 CD20 单抗获 NMPA 批准上市,包括罗氏公司的利妥昔单抗(美罗华)及其 2 款生物类似物——信达生 物公司的达伯华和复宏汉霖公司的汉利康。除此之外,还有罗氏公司的奥妥珠单抗,这也 是首个经糖基化工程结构改造的人源化II型的抗 CD20 单抗。另外,我国神州细胞公司 自主研发的新型抗 CD20 单抗瑞帕妥单抗也于 2022 年 8 月在国内获批上市。鉴于 CD20 的特异性,除针对 CD20 的单抗外,目前已有企业开发出了靶向 CD20 的双抗、ADC、 CAR-T 细胞治疗和合成性 T 细胞受体抗原受体(STAR-T)细胞疗法等,如 Mustang Bio 公司的 CD20 靶向自体 CAR-T 细胞治疗(MB-106)、罗氏和再生元公司等多家药企研发 的抗 CD3/CD20 双抗、特瑞思药业的 CD20 靶向 ADC 药物(TRS005)及乐普生物的 CD20 靶向 ADC 药物(MRG001)等。根据已注册登记的临床研究数据资料,这些正在进行研 究的 CD20 靶向药物主要用于治疗血液肿瘤及多发性硬化症。当下,国内外已有多家企 业布局抗CD20单抗或相关生物类似物的研发,超过110条研究管线正处于临床前期或已 进入临床阶段,同质化竞争比较严重。基于 CD20 靶点的双抗、ADC 和 CAR-T 细胞治疗, 可能成为未来研发的重要方向。
参考资料
- https://mp.weixin.qq.com/s/v9QnhvpCNi-7cTWMURMwrw
- 2022年度中国抗肿瘤新药临床研究评述
