【6.3.3】酶的催化常数(Kcat)
米氏方程里面有2个常数——Km和Vmax。米氏方程外面还有 2个更重要的常数——kcat与kcat/Km
一、kcat–酶催化活性或效率的尺度(A measure of catalytic activity)
kcat就是酶的催化常数,也叫周转数或转换数,即1个酶分子在单位 时间内催化了多少个底物变成了产物
Kcat即酶的催化常数(catalytic constant,Kcat),也就是一种酶的转换数(turnover number),具体是指酶被底物饱和时,每秒钟每个酶分子转换底物的分子数。Kcat可用来衡量一种酶的催化效率。
如果酶遵循米氏方程,则k2 = kcat = Vmax/Et (If the M-M model fits, k2 = kcat = Vmax/Et )
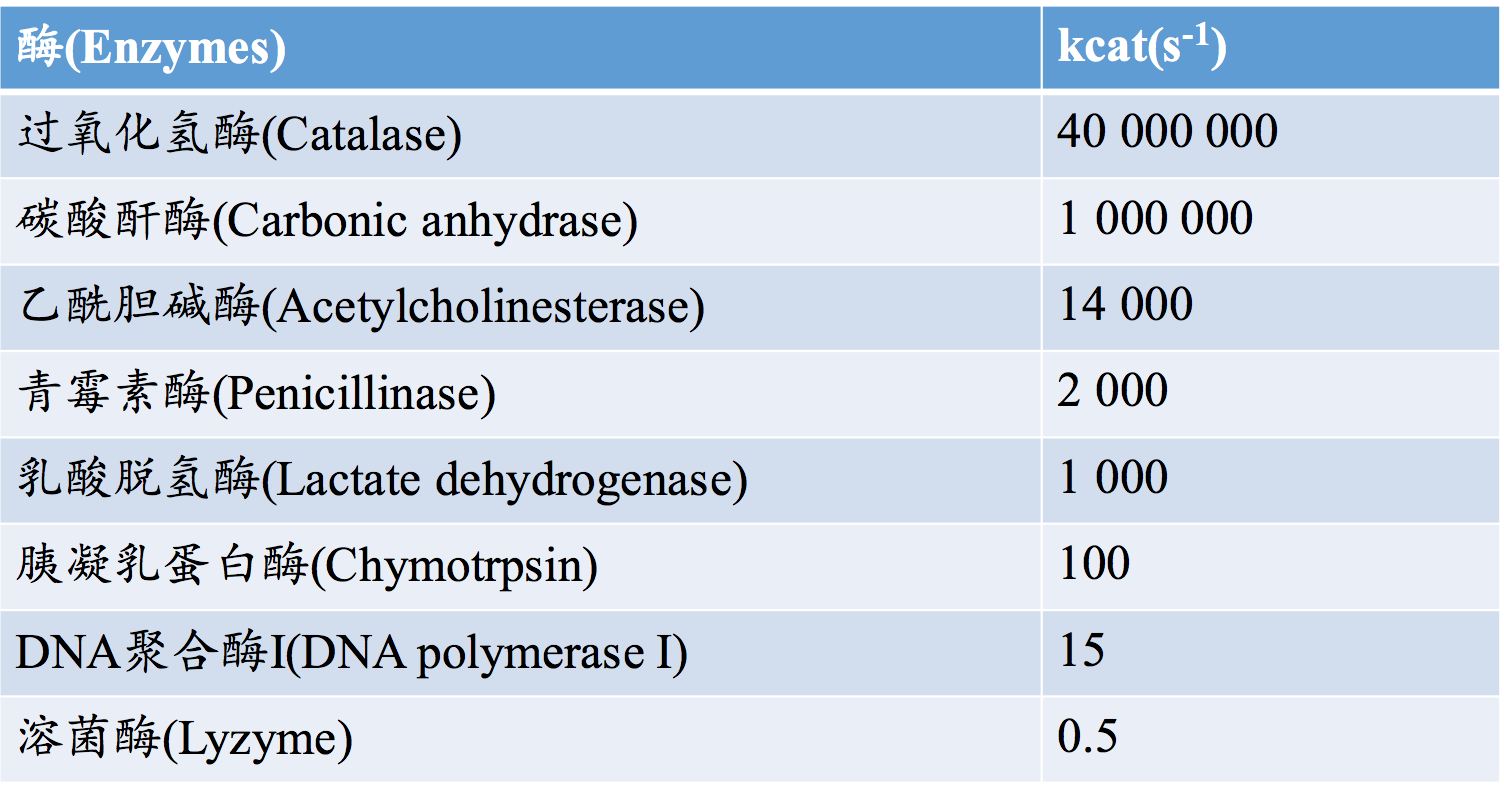
不同的酶的 kcat 大小相差可能很大,小的低于1s-1,大到高于106 s-
几种酶的kcat(Values of kcat for Some Enzymes)
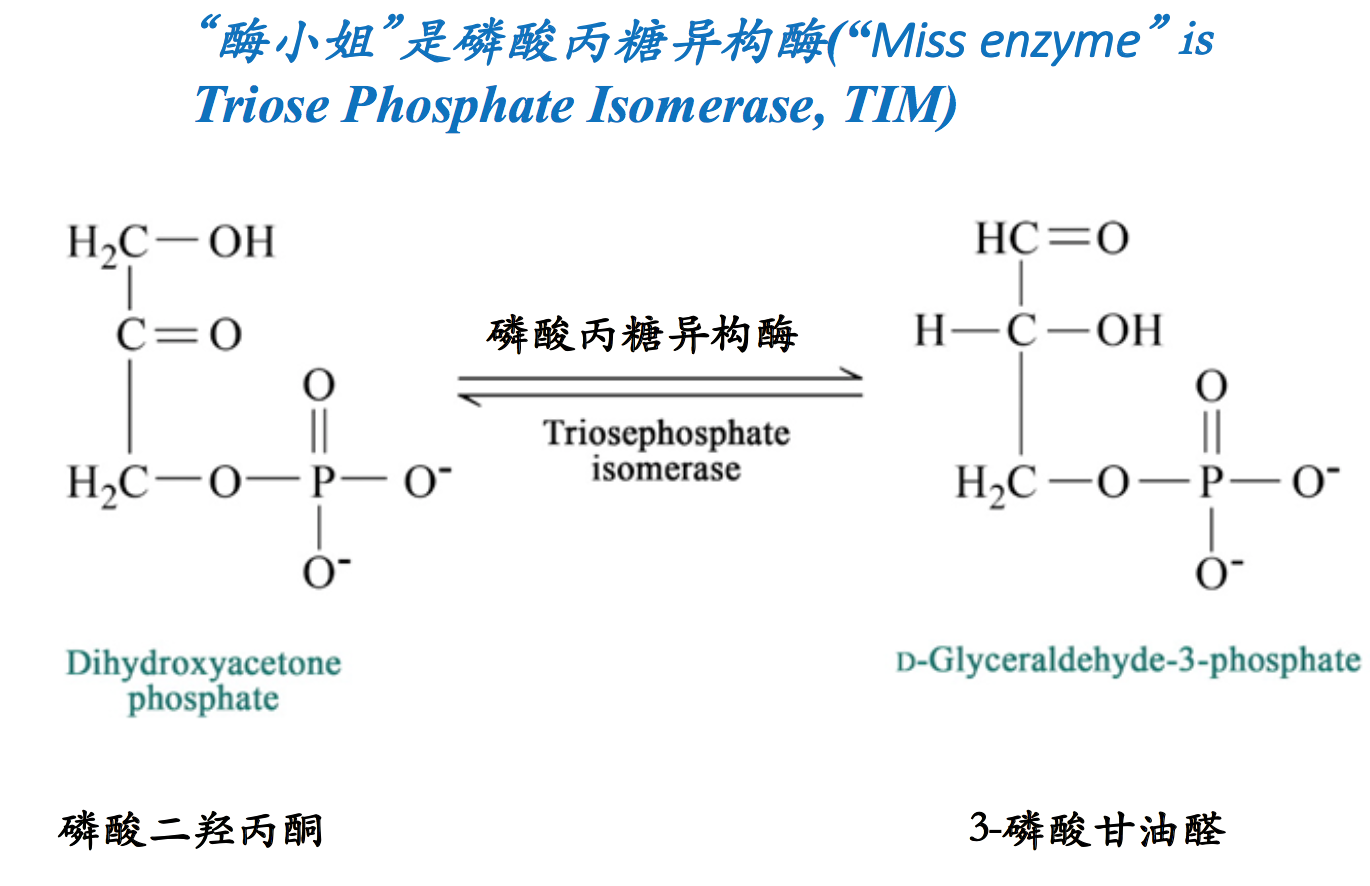
二、kcat/Km–衡量酶完美程度的尺度(An estimate of “how perfect” the enzyme)
- kcat/Km是一个表观二级速率常数(kcat/Km is an apparent second-order rate constant)
- 它显示了底物浓度很低的时候酶如何作用(It shows how the enzyme performs when S is low)
- kcat/Km的上限由底物和酶扩散在一起的扩散系数决定 (The upper limit for kcat/Km is the diffusion limit - the rate at which E and S diffuse together)
几种酶的kcat, Km和kcat/Km(The Values of kcat, Km and kcat/Km for some enzymes)

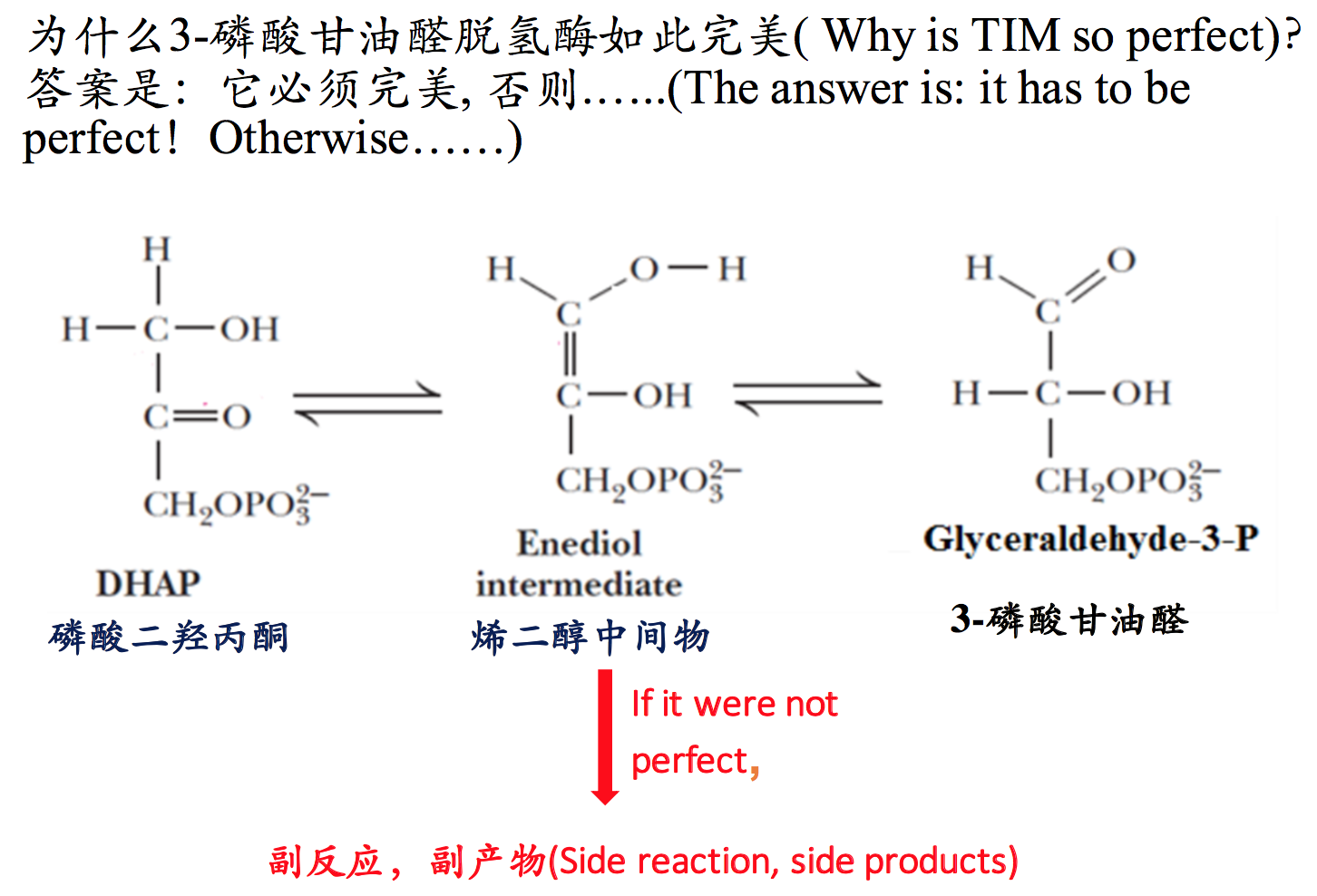
Kcat/Km将Kcat和Km结合在一起,不仅可用来衡量酶的催化效率,还来显示一种酶的完美程度。当[S]﹤﹤Km时,米氏方程可变为v= [E][S]Kcat/Km,这时Kcat/Km表现为底物和酶之间的二级速率常数。该数值表征了在酶足量的情况下,酶的催化表现。同时通过该数值可以比较酶对不同底物的催化效率。
参考资料
- 南京大学 杨荣武老师 《结构生物学》课件
药企,独角兽,苏州。团队长期招人,感兴趣的都可以发邮件聊聊:tiehan@sina.cn
![]() 个人公众号,比较懒,很少更新,可以在上面提问题,如果回复不及时,可发邮件给我: tiehan@sina.cn
个人公众号,比较懒,很少更新,可以在上面提问题,如果回复不及时,可发邮件给我: tiehan@sina.cn

